
脳に潜む「見えない敵」を追え!酸化ストレスと闘うEPRイメージング
脳の中で静かに進行する酸化ストレス……目に見えぬその影響を可視化し、アルツハイマー病の謎に迫る。
北海道医療大学の江本美穂講師が挑む、画期的な「酸化ストレスイメージング」研究が、脳科学の新たな地平を切り拓こうとしている。
EPRイメージング法を駆使し、アルツハイマー病モデルマウスの脳内を探る江本講師。
その鮮明な画像が映し出すのは、これまでには実現してこなかった未知の脳内風景だ。
この研究は、特効薬のない難病の早期発見や新たな治療法開発にどのような光をもたらすのか?
本企画では、江本講師の研究に迫り、酸化ストレスイメージングの現在地と未来図を描く。
避けては通れない加齢により脳の奥底で蠢く「見えない敵」との闘いの最前線に迫るインタビュー。

様々な疾患の原因!?「体の中のサビ」を徹底解明!

―――まずは、研究領域について教えてください。
私の研究を大きく一言で表すと、生体内の酸化ストレスのイメージング研究です。
ただし、現在の研究対象はまだ人間ではなく、いわゆる実験動物における酸化ストレスのイメージング研究に焦点を当てています。
酸化ストレスというキーワードで考えると、様々な疾患との関連が見えてきます。
例えば、糖尿病、アルツハイマー病、脳血管疾患、さらには腎臓障害、肝臓障害、がんなどにおいて、酸化ストレスが非常に大きく関与していることが知られています。
そのため、私の研究手法はこれらの疾患をターゲットにできると考えられます。
現在は特に、アルツハイマー病および、それに関連して老化(エイジング)の研究を行っています。
私が酸化ストレスの研究に携わるようになったきっかけは、実は偶然の出会いでした。
学生時代は主にニューロサイエンス、つまり脳科学や神経科学の分野で学んでいました。
しかし、アカデミックポストを探す段階になったとき、脳をキーワードにしながらも、酸化ストレスの分野でポストを募集していた先生の元へアプライし、この業界に足を踏み入れることになりました。
それから15年以上が経ちましたが、先ほど申し上げたように、アルツハイマー病や脳梗塞などの疾患と酸化ストレスとの関わりが明らかになってきて、私のこれまでの研究と様々な疾患が結びつき、非常に興味深い展開となっています。
さらに、当初は脳にしか注目していませんでしたが、全身の疾患にも知識を広げられる楽しさを感じており、今も酸化ストレス研究に取り組んでいます。
一般的に、病気や疾患というと心臓、腎臓、肝臓といった臓器レベルで捉えがちです。
しかし、酸化ストレス研究ではもっと微視的なレベルに焦点を当てます。
例えば、生体内の脂質やタンパク質、さらにはDNAといった分子レベルでの損傷が研究対象となります。
こうした微小な損傷が積み重なることで、我々が意識できるレベルでの様々な臓器の疾患へとつながっていくのです。
―――「酸化ストレス」という言葉は、よく耳にしますが、ずばりどういうものなのでしょうか?
酸化ストレスは、一般的に「体の中のサビ」と表現されることがあります。
これは複雑な生体のメカニズムを分かりやすく説明するための比喩ですが、実際にはもっと奥深い現象です。
私たち人間をはじめとする多くの生物は、生きるために酸素を必要としています。
なぜなら、酸素を利用してエネルギーを生成しているからです。
この過程は生命維持に不可欠ですが、同時に副産物として活性酸素と呼ばれる物質も生成されます。活性酸素は、一面ではシグナル分子のような働きがありますが、一般的には有害な存在と捉えられています。
しかし、通常の状態では、私たちの体内には活性酸素を除去する仕組みが備わっています。
そのため、普段は呼吸をしてエネルギーを生成しても、特に問題なく生活できるのです。
ところが、何らかの要因でこの除去機能が正常に働かなくなると、生成された活性酸素を消去しきれなくなります。
その結果、活性酸素がDNAやタンパク質、脂質などの生体分子を攻撃し、様々な悪影響を及ぼすことになります。
この状態が、いわゆる「酸化ストレス」です。
酸化ストレスには様々な意味合いがありますが、簡単に言えば、過剰に酸化された状態、あるいはラジカル(不対電子を持つ不安定で反応性の高い分子やイオン)が次々と様々な分子に影響を及ぼしている状態を指します。
本来なら、これらの有害物質を除去する機構が働くはずですが、その機構がうまく機能せず、酸化反応に傾いてしまった状態とも言えるでしょう。
より専門的に捉えると、酸化ストレスとは単に有害物質が過剰に存在することだけを意味するわけではありません。
本来の意味では、有害物質の生成とその除去のバランスが崩れた状態、つまり両者の不均衡を指します。
これはpHでいうと、アルカリ性から酸性に傾いた状態をイメージするとわかりやすいかもしれません。
したがって、私たちの研究では、酸化ストレスの原因を特定することが重要になります。
例えば、有害物質が大量に生成されているために、正常な除去作用が追いつかないのか、それとも有害物質の生成量は通常レベルなのに、除去機能が低下しているために処理しきれないのか。
こうした原因の違いは、疾患によって異なる可能性があります。
そのため、各疾患でどちらが主な原因なのかを突き止め、それに応じた対処法を見出していく必要があると考えています。
予防が最も理想的な目標ー特効薬のない病気の突破口にしたい

―――酸化ストレスは体内がどのような状態になると、生成されるのでしょうか?抑制するために何かできることはあるのでしょうか?
酸化ストレスという言葉は、「酸化」と「ストレス」を別々に捉えるのではなく、一つの統合された概念として理解する必要があります。
つまり、酸化物質が過剰に産生されている状態、あるいはそれを抑制する物質が減少している状態を指します。
この点で、私たちが日常的に経験する仕事上でのプレッシャーなどの精神的ストレスとは異なる概念です。
しかしながら、興味深いことに、そうした精神的ストレスが身体に影響を及ぼし、実際に酸化物質の産生を増加させたり、その消去系の機能を低下させたりすることで、生物学的な意味での酸化ストレス、つまり酸化と抗酸化のバランスを崩すことがあります。
酸化ストレスの抑制方法については、まだ解明されていない部分が多く、その対策は多岐にわたります。
食事や運動など、ライフスタイルの改善によって対処できる面もあります。
一方で、特定の疾患に罹患したことで酸化と抗酸化のバランスが崩れるという、いわば「結果としての酸化ストレス」も存在します。
さらに、紫外線などの外的要因によっても酸化ストレスが亢進することが知られているでしょう。
このように、酸化ストレスは様々な要因が複雑に絡み合って生じるため、その予防には総合的なアプローチが必要です。
具体的には、規則正しい生活、バランスの取れた食事、適度な運動などが挙げられます。
言い換えれば、不規則な生活をしていると、常に酸化ストレスのリスクにさらされていると言えるでしょう。
酸化ストレスの影響は、DNA、脂質(油分)、タンパク質、糖質(糖分)といった小さな分子レベルから始まります。
これらの分子への影響が蓄積されると、最終的には臓器にまで及び、私たちが自覚できる症状や疾患として顕在化し、その影響範囲は驚くほど広範です。
例えば、がんのような全身性疾患、心臓疾患、さらには臓器とは言い難い血液にまで及びます。
また、眼科領域でも酸化ストレスに関連する疾患が見つかっています。
つまり、私たちの体の主要な臓器のほとんどが、何らかの形で酸化ストレスと関わっていると言っても過言ではありません。
酸化ストレスは非常に広範かつ複雑な現象で、日々の生活の中で意識的に予防策を講じることも大切ですが、同時に、さらなる研究の進展が期待されています。
―――現在特に取り組まれている研究について、研究テーマと具体的な内容を教えてください。
現在、私の研究室では、アルツハイマー病モデルマウスを用いた実験を行っています。
このマウスは遺伝子組み換えにより、将来的にアルツハイマー病を発症するよう設計されています。
主な研究目的は、これらのマウスの脳内における酸化ストレスの状態を可視化し、解析することです。
しかし、この研究には一つの大きな課題があります。
現在使用しているモデルマウスは、ある程度の月齢(高齢)になってからアルツハイマー病の症状を発症します。
そのため、観察される現象が純粋にアルツハイマー病に起因するものなのか、それとも単に加齢による変化なのかを区別することが難しいのです。
そこで、私たちはアルツハイマー病と加齢(エイジング)の両方をキーワードに据えて研究を進めています。
これまでの研究で、アルツハイマー病を発症したマウスの脳内では、酸化ストレス状態が有意に変化することが明らかになりました。
さらに興味深いことに、そのようなマウスに運動をさせると、脳内の酸化ストレス状態が改善されるという結果が得られたのです。
この発見は、運動の重要性を裏付ける科学的根拠となり、日常生活に還元しやすいデータとして大変意義深いものでした。
マウスの実験では、普通のケージに数匹のマウスを入れ、餌を与えるだけの環境に、回し車を追加しただけだったのです。
強制的に運動させるのではなく、マウスが自発的に走れる環境を作っただけですが、それでも酸化ストレスは有意に低下しました。
つまり、マウスにとって効果的だったのは日常的な、有酸素運動だったのです。
しかも、マウスが好きな時に好きなだけ動いた結果でした。
ただし、過度な有酸素運動は逆効果になる可能性もあります。
私たちは呼吸によってエネルギーを得ていますが、その代謝の過程で酸化物も生成されます。
したがって、アスリートのような激しい運動ではなく、適度な運動が望ましいでしょう。
運動には血液循環や酸素供給が改善される効果もあります。
体を動かすことは全て脳からの指令によるものですが、仕事で使う頭の使い方と運動で使う頭の使い方は異なります。
そういった意味でも、運動はリフレッシュになるでしょう。
医学的見地からは、アルツハイマー病の早期段階、つまり軽度の認知障害で、酸化ストレスイメージングによって何らかの変化を検出できないかというアプローチを試みています。
アルツハイマー病の特徴的な病理所見であるアミロイドβタンパク質の蓄積が顕著な時期のマウスでは、すでに対照群との有意な差が認められているのです。
しかし、私たちの最新の研究では、実験手法を工夫することで、そのさらに前の段階でも有意な差を見出すことができました。
この早期検出が可能になれば、運動療法や、薬剤ではない食事療法などによって、疾患の進行を抑制できる可能性が開けます。
例えば、酸化ストレスを抑制する有効成分を日常的な餌に混ぜて与え、その効果を検証するという研究にも着手しています。
私たち基礎研究者にとって、アルツハイマー病を完治させることは難しいかもしれません。
しかし、早期に介入することで発症を遅らせたり、進行を緩やかにしたりすることは可能だと考えられます。
それこそが、医師ではない我々研究者にできることなのではないかと思い、今後もこの方向性で研究を深化させていく予定です。
アルツハイマー病研究において、予防は最も理想的な目標です。
確かに、最近新しい薬剤が開発されましたが、他の多くの疾患と同様に、完治や根治に至る治療薬はまだ存在していません。
新薬の効果については、今後の経過を注意深く見守る必要があります。
臨床現場で患者さんと向き合う医師たちも、アルツハイマー病と診断がついた後、他の疾患のように完治させられるかと問われれば、必ずしも肯定的な答えは出せないのが現状です。現段階では、完全な意味での治療薬はまだ存在していません。
そうした現状を踏まえると、発症そのものを予防する、あるいは発症をできる限り遅らせることが、創薬開発以外のレベルで私たち研究者にできる現実的なアプローチではないかと考えています。
そのため、私の研究室では予防的観点からの研究を重点的に進めています。
同時に、私たちが開発した研究システムは、創薬においても重要な役割を果たせると考えています。
例えば、新薬候補のスクリーニング、つまり薬効の検証などに活用していただければと思います。
私たち自身が直接薬を作り出すわけではありませんが、薬の効果を検証する段階で貢献できるはずです。
このように、私たちの研究は二つの方向性を持っています。
一つは、アルツハイマー病にならないための予防法の開発です。
もう一つは、治療薬開発のサポートです。
後者については、薬の効果を検討したり、有効成分を見つけ出したりすることが挙げられます。
例えば、ある成分が病気の進行を抑制できそうだとわかれば、それを論文にまとめて発表します。
そうすれば、創薬研究者がその知見を活用し、新たな薬の開発につなげてくれるかもしれません。
現時点では特効薬のないアルツハイマー病に対し、私たちの基礎研究が、様々なアプローチの出発点や材料として寄与できれば、これ以上の喜びはありません。
史上初!生きたままの状態でイメージングする技術の誕生

―――現在の研究において、直面している主な課題は何でしょうか?
私たちの研究には数多くの課題があります。
その中でも最も大きな課題の一つは、モデル動物の確保です。
現在、研究用のマウスを繁殖させ、成長を待って実験に使用していますが、この過程には様々な困難が伴います。
まず、アルツハイマー病モデルマウスの遺伝的特性について説明しますと、疾患の原因となる遺伝子は父親にのみ存在し、母親には存在しません。
そのため、これらのマウスを交配させても、生まれてくる子マウスのうち、アルツハイマー病の遺伝子を持つ個体は半数以下となります。
言い換えれば、生まれた子マウスの全てが実験に使えるわけではないのです。
さらに、疾患誘発遺伝子を持つマウスは一般的に虚弱で、実験に適した月齢まで成長する前に死亡してしまうことも少なくありません。
こうした要因から、十分な数のモデルマウスを確保することは容易ではないのです。
しかし、研究レベルでの信頼性の高いデータを得るためには、一定数の個体が必要不可欠となります。
仮に1匹のマウスで劇的な効果が見られたとしても、それが偶然の産物である可能性は否定できません。
つまり、ある個体では効果があっても、別の個体では効果がないかもしれないのです。
そのため、同一条件下で多数の個体を用いた実験が求められます。
このように、実験動物を扱う難しさは常に付きまとっているのです。
加えて、私たちが使用している装置にも課題があります。
この装置は市販品ではなく、工学系の共同研究者が開発した特殊なシステムです。
私たちの要望に応じて特化した機能を持つ装置を作っていただいているのですが、そのぶん、不具合が生じた際の対応は容易ではありません。
ただし、この点に関しては、双方向的な研究開発という側面もあります。
つまり、私たちがこの装置を用いて実験データを出すことで、機械の不具合や改良すべき点が明らかになり、それを開発者にフィードバックすることで、さらに優れた装置へと進化させていくのです。
また、イメージング研究においては、単にカメラのようにスナップショットを撮るだけではなく、特殊な薬剤をマウスに投与する必要があります。
市販の薬剤もありますが、新たな機能を持つ薬剤が必要になった場合は、合成薬剤を作れる専門家との共同研究も欠かせません。
このように、私たちの研究は多岐にわたる分野の専門家との連携の上に成り立っており、それぞれの段階で試行錯誤の連続です。
単に「これでイメージングができました」で終わるのではなく、異なる分子での比較検討など、様々な角度からの検証が求められます。
私たちの現在の知見の中でベストな方法を提供したいと考えていますが、その「ベスト」を見つけることが困難を極めるのが現状です。
―――もう一つ現在取り組まれているという、EPRイメージング法についても教えてください。
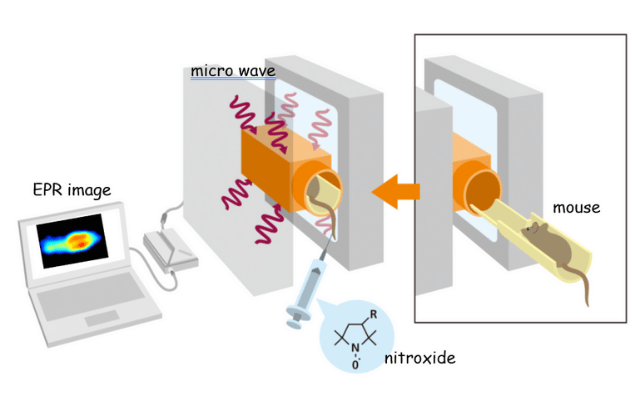
引用:江本研究室私たちが用いている研究手法の根幹をなすのは、EPR(電子常磁性共鳴)イメージングと呼ばれる技術です。
この技術は、皆さんがよくご存知のMRI(磁気共鳴画像法)と原理的に近い部分があります。
MRIが体内の水分子中のプロトンを検出して画像化するのに対し、EPRイメージングでは不対電子、すなわちラジカルと呼ばれる分子が持つ不対電子の空間的分布を可視化します。
この不対電子は、生体内やその他の環境下で様々な相互作用を起こし、最終的には消失していきます。
具体的な実験手順としては、まずマウスの体内に不対電子を持つ薬剤を投与します。
投与直後は、その電子に由来する強いEPR信号が観測されるのですが、時間の経過とともにその信号は徐々に弱まっていきます。
これは、薬剤中の不対電子が生体内の環境によって還元され、失われていくためです。
私たちは、この信号の減衰速度に着目しています。
信号の減衰が遅い領域は酸化ストレスが亢進している可能性が高く、逆に速い領域では酸化ストレスの程度が比較的低いと考えられます。
こうした情報を空間的に統合することで、生体内の酸化ストレスの分布を画像として捉えることができるのです。
このように、どの部位で酸化還元反応が活発に起こっているかという空間的情報を得られることが、イメージング技術の大きな強みだと思います。

▲EPRイメージング装置酸化ストレス研究の歴史は長く、現在も多くの研究者がこの分野で活躍していますが、その多くは臓器や組織の一部、血液サンプル、培養細胞などを用いた、いわゆるin vitro(試験管内)の研究でした。
つまり、生きたままの状態でイメージングする技術は、ほとんど存在しなかったのです。
確かに、サンプルを採取して特定の成分の発現量や活性を調べ、DNA、タンパク質、脂質などの分子レベルでの詳細な分析は、現在でも盛んに行われており、細胞レベルのイメージングも存在します。
しかし、私たちが取り組んでいるような、生きた個体レベルでの酸化ストレスイメージングは、世界的に見ても稀有な技術だと言えるでしょう。
生きた個体の中で起こっている現象を、リアルタイムで、しかも視覚的に一発で捉えられる技術は、このEPRイメージング以外には存在しません。
この点こそが、私たちの研究の独自性であり、大きな強みとなっています。
一歩踏み込んで知る勇気ー出来ることから始めよう!

―――5年後、10年後といった将来、このイメージング技術に何を期待されていますか?また、酸化ストレスイメージングが医療業界や医療現場にどのような影響を与えると予想されますか?
まず、医療現場への貢献という観点から見ると、やや楽観的かもしれませんが、健康診断などのスクリーニング検査の一環として、酸化ストレス評価が広く用いられるようになることを期待しています。
様々な疾患に酸化ストレスが関与していることを考えると、どこかに病気の兆候がないかを探る手段として、酸化ストレス検査が一般化されれば理想的です。
次に、研究レベルにおいては、この手法を用いる研究者が増えることを願っています。
私自身は現在、脳に焦点を当てた研究を行っていますが、最近になって腎臓や肝臓など、他の臓器も観察可能なシステムが開発されました。
今後、様々な疾患に対してEPRイメージングを応用する研究者が増えれば、この分野の発展に大きく寄与するでしょう。
さらに言えば、医療に関わる人々が誰でも簡単に使えるようなシステムになれば、非常に素晴らしいことだと思います。
酸化ストレスイメージング研究の未来のためには、他分野との連携が不可欠です。
私たちの研究は主に個体レベルでの変化を追っており、分子メカニズムの解明には直接取り組んでいません。
しかし、このイメージング技術をきっかけに、分子レベルの研究をされている先生方との共同研究が進めば、より包括的な理解が得られるはずです。
つまり、私たちが個体レベルでの大きな変化を捉え、共同研究者がミクロの視点から詳細を明らかにする、そうした相補的なアプローチが理想的だと思います。
なぜなら、分子レベルでポジティブな結果が得られたとしても、それが必ずしも個体レベルでも同様の効果をもたらすとは限らないからです。
ミクロからマクロまで、シームレスに研究を進められれば、最も効果的な成果が得られるでしょう。
―――今後先生が挑戦していきたいことは何でしょうか?
分子レベルの研究は技術的にも知見の面でも進歩が非常に早く、私たちもその進歩から多くを学べると考えています。
そのため、まずは共同研究という形で参画させていただくのが最適だと思います。
もちろん、新たに独自の研究を立ち上げるという選択肢もありますが、そうなると完全にゼロからのスタートとなり、いわば学生レベルから始めることになってしまうのです。
それよりも、現在進行中の研究プロジェクトに共同研究者として加わらせていただく方が、研究の進捗も早くなるでしょう。
理想を言えば、すべてを自分たちの研究室で完結できれば素晴らしいのですが、近年の研究レベルや進め方、そして生み出されるデータの膨大さを考慮すると、一つの研究室だけで何かを成し遂げるのは難しくなってきています。
そのため、私たちの研究に興味を持っていただける先生がいらっしゃれば、ぜひ一緒に研究を進めさせていただきたいと常々考えているんです。
単独の研究室で全てを担うには限界があり、多様な研究を行えば行うほどデータ量も増大になり、一つの研究手法だけで何かを主張することは困難になってきます。
また、これもやらなければならない、あれもやらなければならないと研究テーマが増えていくと、それぞれの分野に特化した専門家の存在が不可欠になります。
そうすることで、様々なアプローチから多角的に現象を観察し、理解することができるのです。
理想を言えば、そうした多角的な視点から一つの結論を導き出せれば最高です。
その意味で、EPRイメージングはそうしたアプローチの一つとして位置づけられるでしょう。
今後、新たな研究手法を開拓していく上でも、他の研究領域の専門家とコラボレーションできれば、それが最善の道筋になると確信しています。
―――最後に、読者の皆様にメッセージをお願いします!
現状では、私たちの研究は動物実験のレベルにとどまっていますが、将来的には生体応用の分野で人のサンプルを研究に使いやすくなったり、より臨床に近い研究ができる環境が整うことを願っています。
そのためには、社会的、法律的な面も含めた環境づくりが必要不可欠です。
新しい研究分野の存在や可能性を広く知っていただき、それらを積極的に活用していくべきだという声が上がることを期待しています。
私たちのデータは現在マウス実験に限られていますが、これをさらに実臨床に近いレベルまで引き上げていきたいと考えてます。
そのためには、様々な分野の垣根を越えて幅広い知識を共有し、多様な場面で活用していくことが重要になります。
上層部の理解と行動、そして社会全体の声が大きな推進力になるでしょう。
ここで強調したいのは、新しいことに対する好奇心と、それを理解しようとする姿勢の大切さです。
「わからない」で片付けるのではなく、「なんだろう」と思い、知ろうとする、今回のようにお話を聞いて少し理解が深まると、それが明日の行動や新たな話題につながるかもしれません。
口コミのように、どこかでつながっていけばいいなと思います。
すぐに大きなことを立ち上げる必要はありません。何かを見て、興味を持ち、知るだけでいいのです。
その行為自体が何かを変えるかもしれない種となります。私たちはその種を撒き続けたいと考えています。
新しい技術や知見に興味を持ち、それらについて学び、日常生活に取り入れていってください。
一人一人の小さな行動が、私たちの研究を前進させ、ひいては社会全体の健康増進につながっていくのです。

はい
25%
いいえ
75%
はい
25%
いいえ
75%








